用數據,辨清事實。 關鍵詞:COVID-19;二價疫苗; 導言: 自COVID-19大流行以來,盡管治療藥物、疫苗和單克隆抗體不斷被開發,但隨著其變體的不斷出現,仍然伴隨著高感染率和死亡率。 找到能降低重症風險、不易產生病毒耐藥性的新型預防類藥物,已經刻不容緩! 但新藥研發談何容易? 在已經過臨床檢驗的上市藥物中找到能夠治療COVID-19的候選藥物,無疑將是更有高效的策略。 新冠病毒感染宿主時
用數據,辨清事實。
關鍵詞:COVID-19;二價疫苗;
導言:
自COVID-19大流行以來,盡管治療藥物、疫苗和單克隆抗體不斷被開發,但隨著其變體的不斷出現,仍然伴隨著高感染率和死亡率。
找到能降低重症風險、不易產生病毒耐藥性的新型預防類藥物,已經刻不容緩!
但新藥研發談何容易?
在已經過臨床檢驗的上市藥物中找到能夠治療COVID-19的候選藥物,無疑將是更有高效的策略。
新冠病毒感染宿主時結合的受體至關重要,也是簽字的治療靶點。
其中,血管緊張素轉換酶2(ACE2)尤其引人注目,ACE2是一種跨膜羧肽酶,具有廣泛的底物特異性,包括血管緊張素II(SARS-CoV-2的主要受體),它能直接結合不同冠狀病毒的刺突蛋白,對SARS-CoV-2具有高親和力。
因此,COVID-19主要影響表達ACE2的組織,例如肺、心血管係統、消化道和膽道係統,那麼改變ACE2的表達則可以阻止病毒感染宿主。
但目前問題在於人們對於如何調節ACE2表達尚不清楚。

2022年12月,英國科學院在Nature雜誌發表了題為“FXR inhibition may protect from SARS-CoV-2 infection by reducing ACE2(FXR抑製可通過減少ACE2來防止SARS-CoV-2感染)”的研究論文,為臨床“老藥新用”更快速找到治療COVID-19的藥物提供了非常重要的思路。
1)研究者首先使用人膽管細胞類器官來證明膽汁酸受體法尼醇X受體(FXR)可以調控ACE2表達,且這一機製適用於多種受SARS-CoV-2影響的組織。
2)研究者進一步證明利用獲批藥物熊去氧膽酸(UDCA)或非處方植物甾體(ZGG)抑製FXR信號,可以減少ACE2表達和SARS-CoV-2感染。
3)最後,研究者用回顧性登記數據確定了UDCA治療與SARS-CoV-2感染後陽性臨床結果之間的相關性,並在肝移植受者的獨立驗證隊列中證實了這些發現。
由此,這項工作確定了FXR在控製ACE2表達方麵的新功能,並提供證據表明調節該通路可能有利於減少SARS-CoV-2感染,為未來的臨床試驗鋪平道路。
課題的設計和主要結果
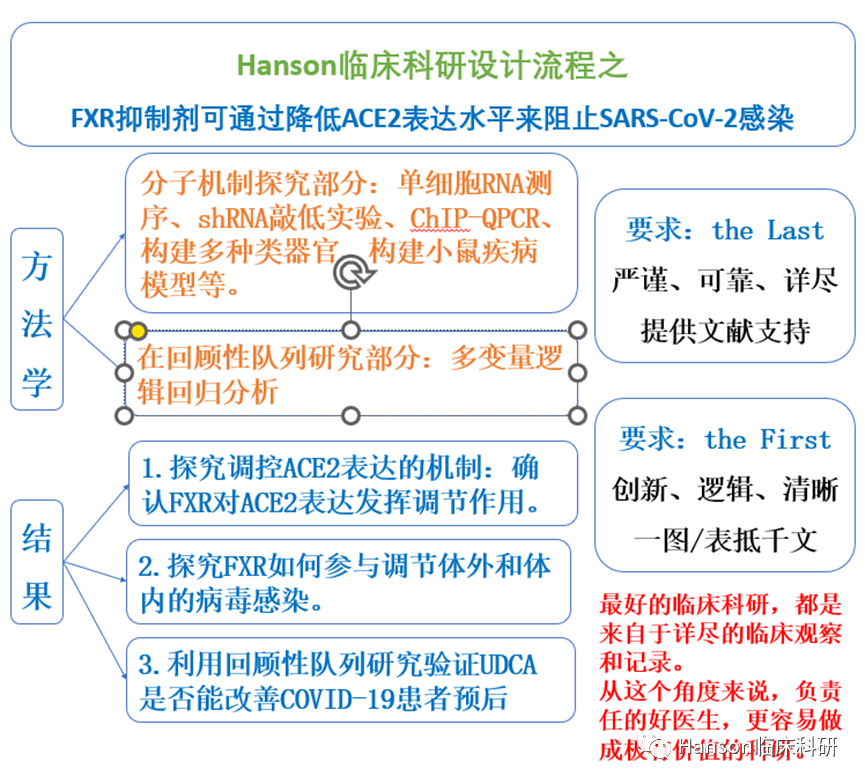
我們通過對原文的設計和結果進行重新總結和整理,提取對臨床醫生有幫助的研究思路。這項研究的設計非常簡單,如下麵的流程圖所示。主要結果
1)探究調控ACE2表達的機製
考慮到膽管細胞中ACE2的高表達,研究人員首先利用膽管細胞類器官(CO)作為原理驗證係統來探究調控ACE2表達的機製。需要注意的是,作者發現膽汁酸(CDCA)對於ACE2的表達至關重要。由於CDCA是膽汁酸受體和轉錄因子FXR最有效的天然激動劑,作者假設CDCA可以通過FXR控製ACE2表達。為了驗證這一點,作者利用shRNA敲低膽管細胞類器官中的FXR,與預期一致,阻止了ACE2的上調,緊接著,作者利用ChIP-QPCR(染色質免疫沉澱)確認FXR可以直接結合在ACE2的啟動子區域以調節器轉錄活性。不限於膽管細胞,作者還觀察到包括呼吸道和腸上皮類器官中FXR對ACE2表達的調節作用。
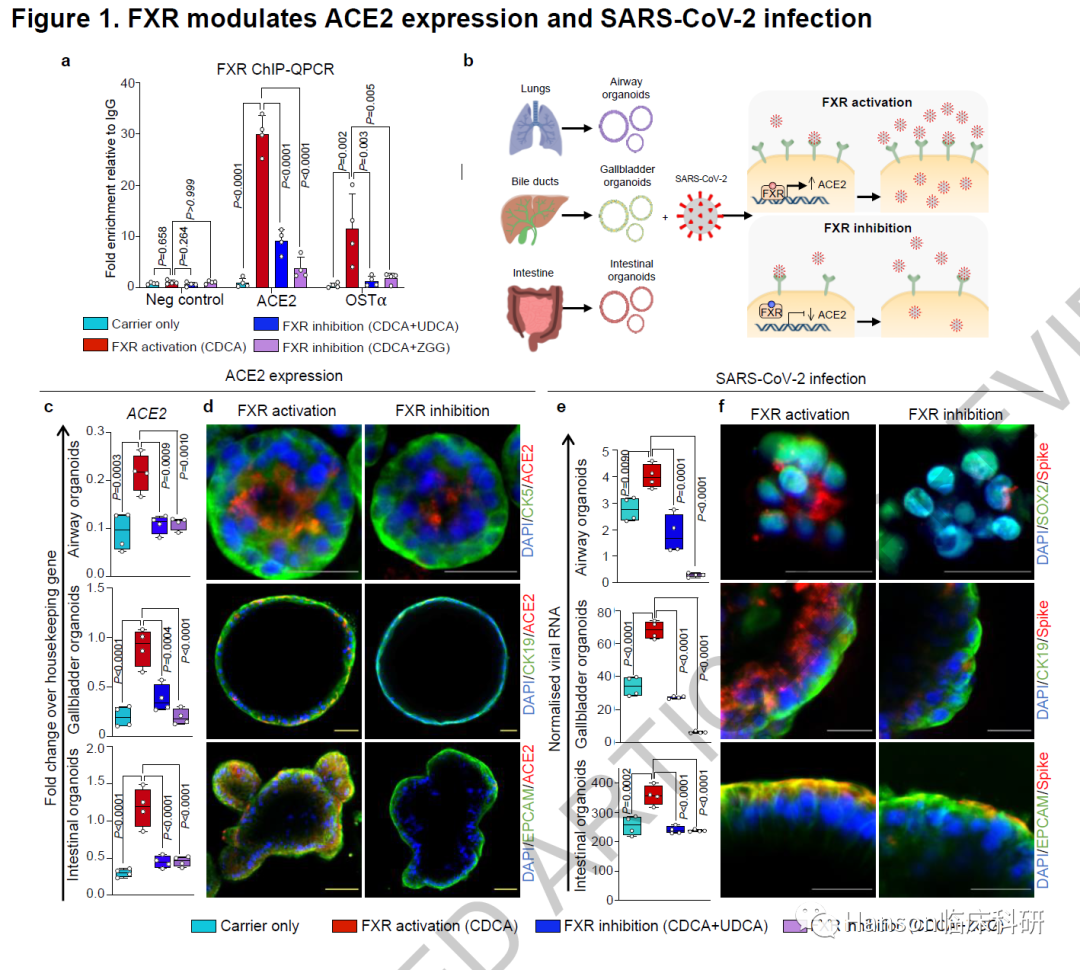
圖1. FXR調節ACE2表達並影響SARS-CoV-2的感染。
2)FXR參與調節體外和體內的病毒感染
基於上一部分的研究結果,他們想進一步探究FXR介導的ACE2下調是否可以降低體外或體內係統對SARS-CoV-2感染的易感性。
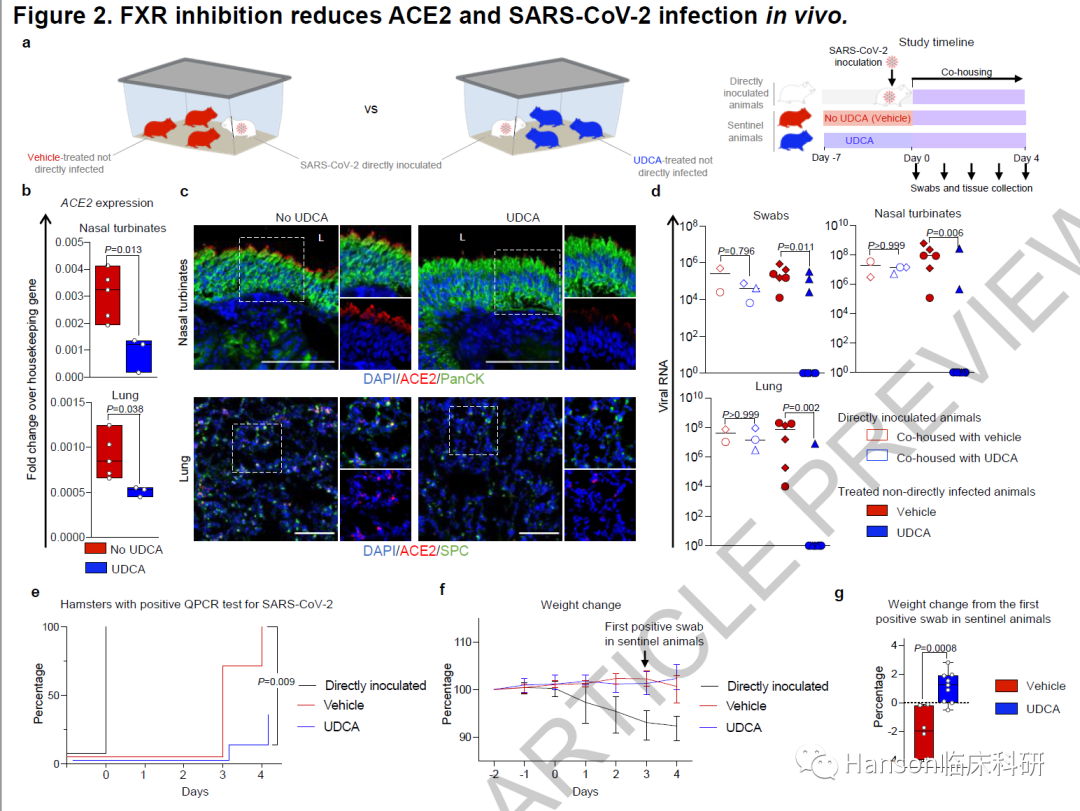
首先,作者取不同類器官分別在存在或不存在UDCA或ZGG(可抑製FXR信號)的情況下,用從患者鼻咽拭子中分離出的SARS-CoV-2感染它們。結果顯示,兩種藥物均可降低三種類器官的感染。那麼這種效果是否可以在體內複現?作者進一步評估了兩種藥物對感染SARS-CoV-2小鼠的影響。相較於對照組的100%感染,UDCA治療後9隻中有6隻未能感染,且剩餘感染的3隻症狀較輕。
圖2.抑製FXR可減少體內ACE2和SARS-CoV-2感染。
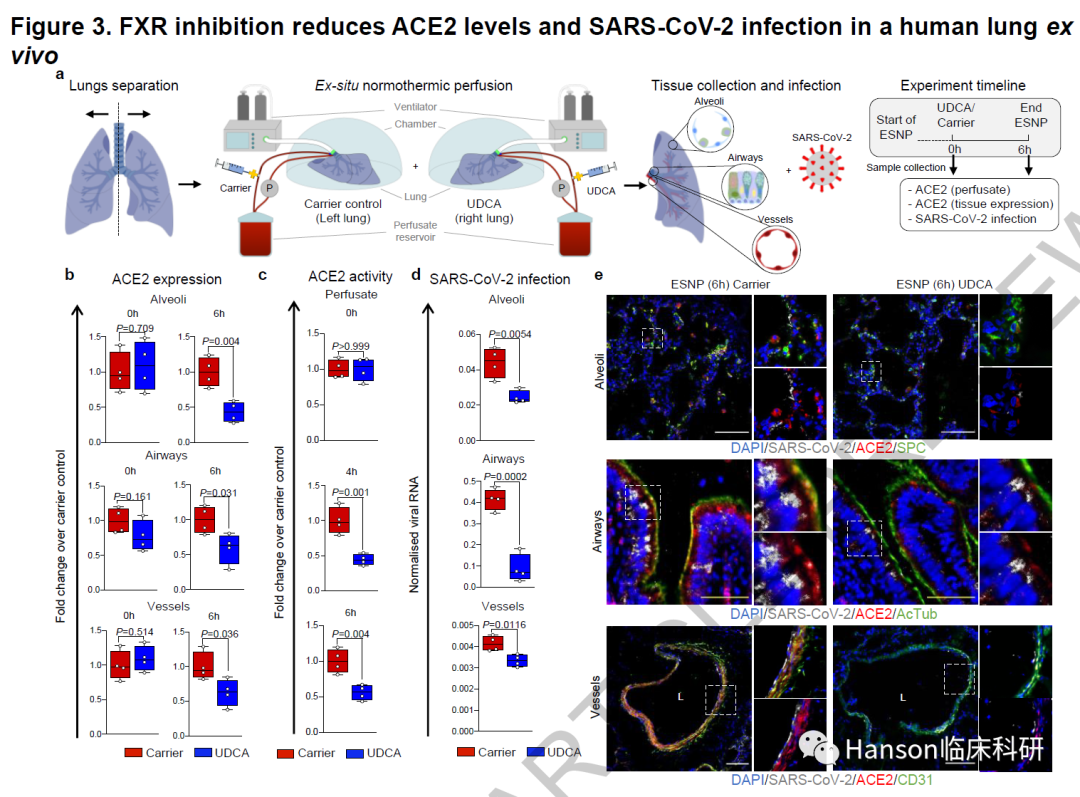
當然,最重要的還是能看到在人類器官中真實的呈現這些效果。為此,研究人員對一對離體人肺進行處理(左右肺分別為對照組和UDCA處理組),用UDCA離體治療降低了肺實質、氣道和肺血管中的ACE2表達以及灌注液中的ACE2活性,並且減少了SARS-CoV-2感染。圖3.抑製FXR可降低人肺體外ACE2水平和SARS-CoV-2感染。
3)UDCA可能會改善COVID-19患者預後
基於這些觀察,研究人員進一步探索UDCA治療對COVID-19患者預後的潛在影響,於是他們分析了COVID-Hep/SECURELiver登記情況(包含COVID-19的慢性肝病患者n=1096,接受UDCA的膽汁淤積性肝病患者n=31),其中,接受UDCA的患者與未接受者相比有更好的結果,包括住院率、ICU入住率和死亡率。
研究人員試圖在第二個獨立的患者隊列中重新這些結果,於是分析了VOCAL隊列中的肝移植接受者,他們至少接受了兩劑COVID 19 mRNA疫苗,其中有24例正在接受UDCA治療,其餘的72例未接受。結果顯示,接受UDCA治療的患者發生中度、重度或危重症的可能性較小,在多變量邏輯回歸中,UDCA暴露與46%的COVID-19發病幾率降低相關。綜上所述,這些發現支持在大型前瞻性臨床試驗中進一步研究UDCA對COVID-19臨床結果的影響。
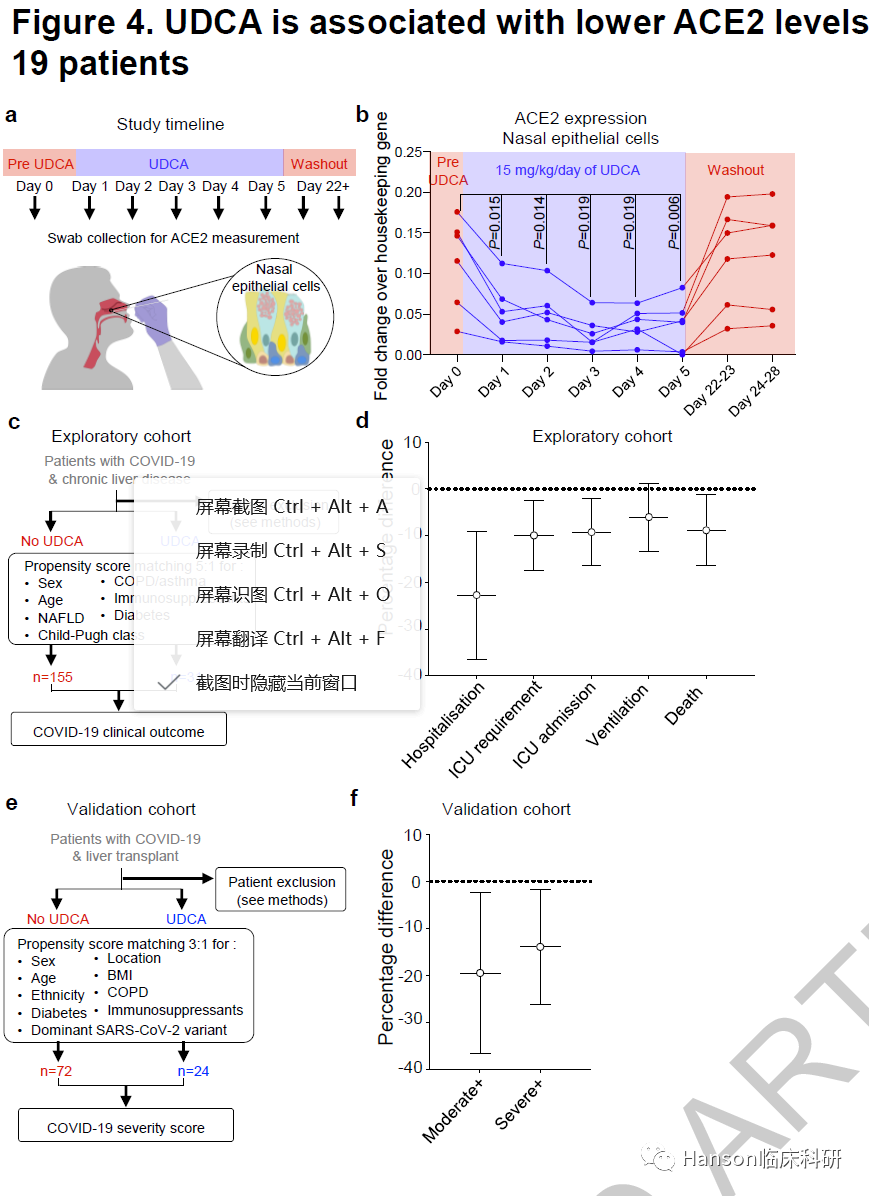
圖4.在COVID-19患者中,UDCA與較低的ACE2水平和較好的臨床結果相關。
主要結論
這項工作表明靶向ACE2作為COVID-19治療策略的潛力,可以作為藥物開發的合理候選。
ACE2作為藥物靶點具有幾個優勢:
①它是宿主導向治療,不針對病毒,ACE2是病毒進入細胞的關鍵,因此對於不斷變異的病毒來說,這種療法更具有彈性;
②ACE2是多種冠狀病毒的共同受體,例如SARS CoV和HCoV-NL63,這一策略可能會在未來冠狀病毒爆發時提供快速部署的幹預措施。
基於ACE2的上述特點,本研究確定的UDCA就是一種非常有吸引力的ACE2調節劑:
①可以分別在體外類器官、體內動物模型和人器官上降低SARS-CoV-2感染率;
②降低重症率;
③耐受性好和副作用小,強調了其在弱勢群體中作為藥物預防SARS-CoV-2感染的可行性。、
編者按:
從科研上看,這項研究之所以發表於Nature這一頂級期刊,主要因素包括:
1.基於詳盡的分子機製為靶向ACE2和UDCA的進一步驗證提供了紮實的理論基礎;
2.研究手段多樣:單細胞RNA測序、shRNA、ChIP-QPCR、類器官、小鼠模型,以及回顧性隊列研究等。
對應臨床應用,更有局限性:
該研究不是臨床試驗,因此不能排除混雜和選擇偏倚的可能性。因此,必須在前瞻性雙盲臨床試驗中驗證這些結果,並全麵評估該藥物對ACE2水平和SARS-CoV-2感染易感性的影響。
copyright©醫學論壇網 版權所有,未經許可不得複製、轉載或鏡像
京ICP證120392號 京公網安備110105007198 京ICP備10215607號-1 (京)網藥械信息備字(2022)第00160號