全球65歲以上人口的比例正在迅速增長,由於阿爾茨海默氏症、帕金森氏症和肌萎縮側索硬化症 (ALS)等神經退行性疾病都與衰老有關,因此患有這些疾病的病例數量正在大大增加。據估計,目前世界上有 5500 萬人患有癡呆症,預計到 2050 年全球將有 1.39 億人患有癡呆症。盡管全世界的科學家和製藥公司都做出了巨大努力,但仍然沒有針對阿爾茨海默病的疾病緩解療法(AD)。 現已有 20 多項研究表明,
全球65歲以上人口的比例正在迅速增長,由於阿爾茨海默氏症、帕金森氏症和肌萎縮側索硬化症 (ALS)等神經退行性疾病都與衰老有關,因此患有這些疾病的病例數量正在大大增加。據估計,目前世界上有 5500 萬人患有癡呆症,預計到 2050 年全球將有 1.39 億人患有癡呆症。盡管全世界的科學家和製藥公司都做出了巨大努力,但仍然沒有針對阿爾茨海默病的疾病緩解療法(AD)。
現已有 20 多項研究表明,減少大腦中的澱粉樣蛋白無助於顯著改善AD患者的臨床結果。近日抗澱粉樣泛白抗體Crenezumab宣布臨床試驗失敗,與Aducanumab 一起,成為未能提供臨床益處的AD治療試驗中的最新案例。Lecanemab 是一種針對聚集的可溶性和不溶性澱粉樣蛋白 β 的人源化免疫球蛋白 γ1 (IgG1) 單克隆抗體,也被證明具有有限的認知益處。但是與這些藥物相關的腦水腫、出血和死亡風險也令人擔憂,它們的使用需要仔細監測、基因檢測和排除疑似腦澱粉樣血管病或服用抗凝劑的患者。這些令人失望的治療進展可能掩蓋了大話對微生物群在阿爾茨海默病分子機製中的作用的理解的最新進展。
微生物群在AD和帕金森氏病 (PD)和ALS等相關神經變性中的關鍵作用最近得到證實。所有這些病症的主要特征包括聚集蛋白(例如 AD 中的澱粉樣蛋白β蛋白和 PD中的α突觸核蛋白)的沉積、大腦中免疫係統的激活以及活性氧分子的存在,這些分子是不穩定的、具有高反應性和破壞性的。腸道中的微生物群通過不同的分子機製影響所有這些過程。


1、微生物澱粉樣蛋白
鼻子、嘴巴和腸道中的微生物會產生功能性細菌澱粉樣蛋白,這些蛋白已被證明會導致大腦中神經元蛋白的模板化交叉接種,從而加速神經退行性疾病模型中的大腦澱粉樣蛋白沉積。研究表明,微生物群會產生可能參與神經變性的功能性澱粉樣蛋白,研究者已經在大鼠中記錄了澱粉樣蛋白通過迷走神經從腸道進入大腦這一過程。此外,全基因組篩選數據表明,由大腸杆菌和其他細菌製成的功能性細菌澱粉樣蛋白與神經元內的神經元澱粉樣蛋白共定位,通過交叉接種促進聚集,並在 AD、ALS 和亨廷頓舞蹈症的動物模型中促進疾病進展。
此外,腸道中的功能性細菌澱粉樣蛋白被先天免疫係統識別為與病原體相關的分子模式,這已被證明會增加大腦中對神經元澱粉樣蛋白的免疫反應並加重功能缺陷。功能性細菌澱粉樣蛋白激活Toll樣受體1和2、NFkB和iNOS通路,導致神經炎症和氧化毒性增強,這是大腦免疫係統識別神經元澱粉樣蛋白的類似途徑。並且,大腦中先天免疫係統的激活促進啦 AD模型小鼠中澱粉樣蛋白的聚集。

微生物群在AD治療中的潛力
鑒於微生物種群對神經退行性疾病的影響,我們可以推測出,通過微生物種群對調整可以實現對AD等神經退行性疾病的調節。因為人體腸道內的微生物種群可以通過飲食顯著改變。研究表明,人類在短短2周內改變飲食可以顯著改變腸道細菌種群的性質,從而對健康產生有益影響。這種通過改變飲食來改善健康的努力可以稱為“廚房基因療法”,因為飲食的改變會改變我們體內的細菌群落。
討論
全球範圍內許多研究者正在努力開發能夠影響腸道微生物群及其代謝產物並有益於人類健康的藥物
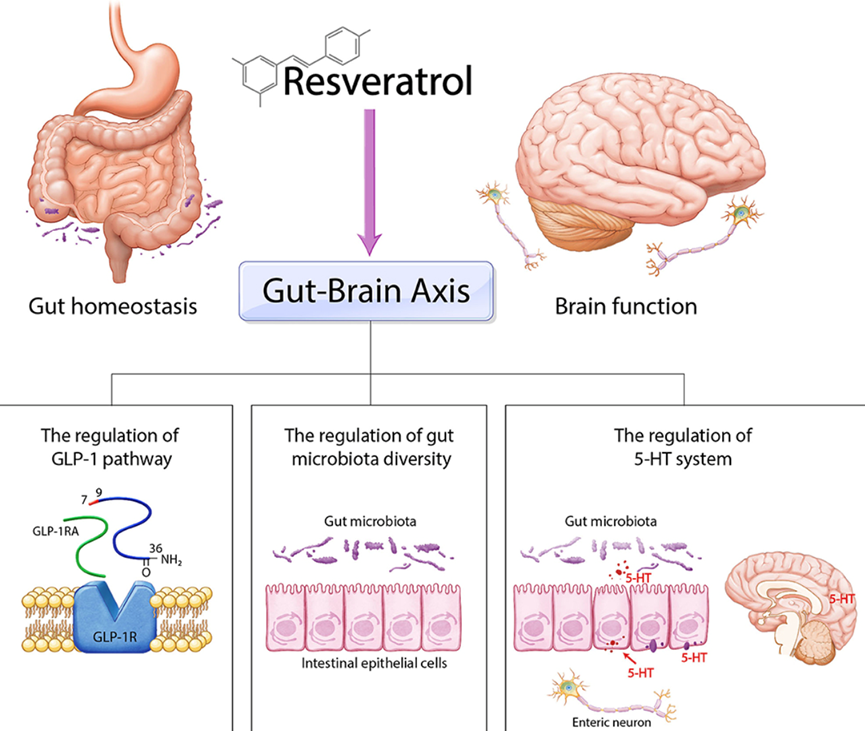
這些將會有影響腸道細菌的藥物為大腦提供益處,並不需要藥物本身進入血液或穿過血腦屏障。探索這種治療方法有許多潛在作用途徑:益生菌提供活菌;益生元為理想的細菌提供食物。此外,眾所周知抗生素對腸道細菌也有很大的影響。也有研究正在探索細菌移植的方法,開發改變細菌代謝對健康有益的藥物。例如,桑普森等人表明,口服攝入具有抗澱粉樣蛋白作用的多酚對帕金森模型小鼠的行為具有有益影響。也有研究報告了多酚白藜蘆醇對腸腦軸具有明顯的影響,並對AD等神經退行性疾病結局具有良性改善。
參考文獻
Friedland RP and Haribabu B (2023) Neurodegenerative diseases: from gut-brain
axis to brain microbiome.Front. Aging Neurosci. 15:1171955.doi: 10.3389/fnagi.2023.1171955
copyright©醫學論壇網 版權所有,未經許可不得複製、轉載或鏡像
京ICP證120392號 京公網安備110105007198 京ICP備10215607號-1 (京)網藥械信息備字(2022)第00160號